|
? 필요한 것은
페트 병(1.5ℓ 짜리), 구부러진 빨대, 투명한 유리병, 모래 약간, 송곳, 고무 찰흙 약간. 마그네슘
리본(학교에서 거래하는 과학사에서 구입 가능), 나무 젓가락
? 어떻게 할까요?
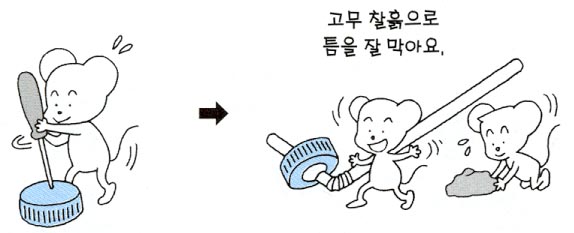
1. 페트 병의 뚜껑에 송곳으로 구멍을 뚫는다.
2. 구부러진 빨대를 끼우고 고무 찰흙으로 틈새를 막는다.
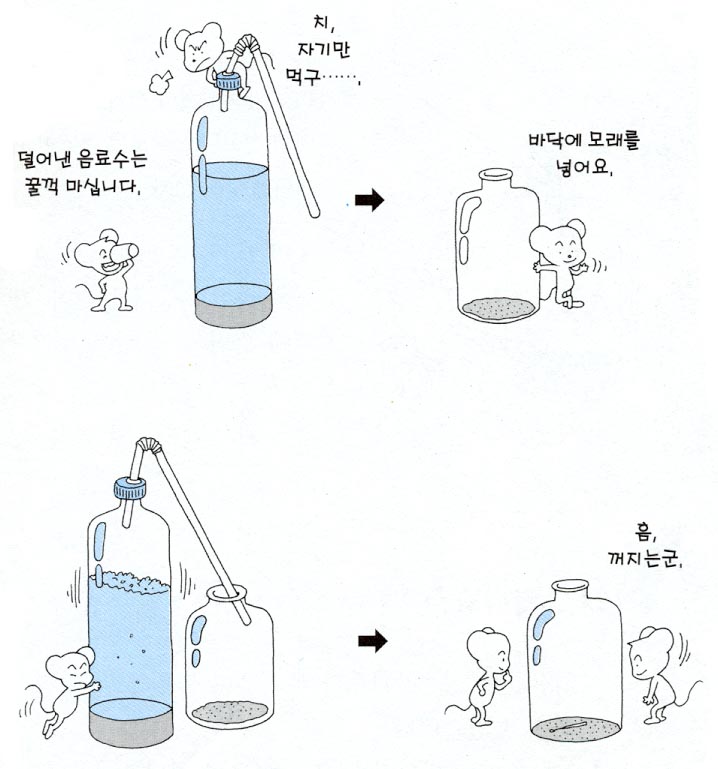
3. 음료수를 1/4정도 덜어내고 뚜껑을 끼운다.
4. 투명한 유리병 바닥에 약간의 모래를 넣는다.
5. 음료수를 좌우로 흔들면서 이산화탄소 기체를 발생시켜 투명한 유리병에 모은다.
6. 이산화탄소가 모아진 투명한 유리병에 성냥 깜부기불을 넣어 불이 꺼짐을 확인하여 보자.
|
|
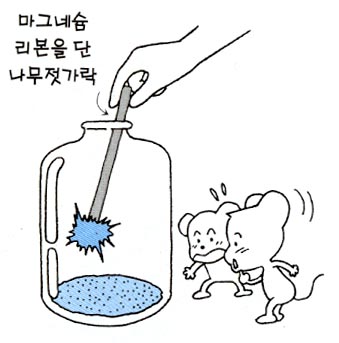
7. 마그네슘 리본을 약간 잘라 나무 젓가락에 고정시켜 불을 붙여 이산화탄소를 모은 투명한 유리병에 넣어
보자.
★ 마그네슘 분말을 풀과 혼합하여 종이로 둥글게 말아 햇볕에 말린 다음 나무 젓가락에 묻혀 연소시키면 꽤 오랫동안
연소 반응을 볼 수 있다.
|
|
? 왜 그럴까요?
이산화탄소는 공기보다 무거우며 불을 끄는 성질을 가지고 있습니다.
그런데 우리는 위의 실험을 통해 이산화탄소가 모아진 투명한 유리병에 불이 붙은 마그네슘 리본을 넣으니까 불이
꺼지는 것이 아니고 오히려 빛을 더 내면서 잘 타는 현상을 보게 됩니다. 어떻게 이런 일이 일어날 수 있을까요?
이산화탄소(CO2)는 2개의 산소와 1개의 탄소가 결합되어 있습니다. 다른 물질들은 이산화탄소
속에서 탈 수가 없지만 마그네슘은 탄소와 산소가 결합된 이산화탄소 중의 산소를 빼앗아 활발하게 타는 것입니다.
이산화탄소는 불을 끄는 성질을 가지고 있기 때문에 모든 물질들을 태울 수 없는 것으로만 생각하셨겠죠?
하지만 이번 실험으로 마그네슘처럼 화학적으로 반응이 활발한 물질은 이산화탄소 속에서도 연소할 수 있다는 사실을
확인할 수 있었습니다.

| | 



